Popis
Rybí olej s organicky viazaným jódom
Rybí olej s organicky viazaným jódom poskytuje dvojakú výhodu, zabezpečuje vysoko vstrebateľnú a biologicky využiteľnú formu jódu a zároveň dodáva telu esenciálne omega-3 mastné kyseliny. Rybí olej ako liečba má pre telo niekoľko pozitívnych vlastností.
U žien môže rybí olej znižovať citlivosť estrogénových receptorov, vhodný preto môže byť pri fibrocystickom ochorení prsníka a vaječníkov. Antiproliferatívne účinky organicky viazaného jódu môžu vo veľkej miere obmedzovať nadmerné delenie buniek pri vytváraní cýst. Organicky viazaný jód tak môže vysoko napomáhať pri liečbe rakoviny u oboch pohlaví, môže tiež napomáhať brániť nadmernému nekontrolovateľnému deleniu buniek. Omega-3 mastné kyseliny pôsobia synergicky, protizápalovo.
Ďalšie účinky rybieho oleja sú, že pri zníženej funkcii štítnej žľazy môže vysoko pomáhať zvyšovať tvorbu tyroxínu a tým znižovať dávky náhradného hormónu, prípadne v začiatočných štádiách úplne sa vyhnúť potrebe podávania náhradného syntetického hormónu. Odporúčaný je preto pri zápaloch štítnej žľazy s prejavmi hypertrofie = zväčšenia.
Jód je nevyhnutný pre funkciu všetkých žliaz, tvorbu tráviacich štiav, slín a sĺz. Nedostatok jódu rovnako ako aj omega-3 mastných kyselín môže viesť k syndrómu suchého oka. Obe výživové zložky prípravku pôsobia synergicky – spoločne v prevencii a podpornej liečbe syndrómu suchého oka. Napomáhajú obmedzovať zápaly očí, chrániť očnú sietnicu, zlepšovať produkciu slzného filmu a zvyšovať jeho hydrofilno-lipofilnú stabilitu.
Dávkovanie: Dospelí 1 čajovú lyžičku (2,5ml) denne s jedlom, pri ochoreniach polievkovú lyžicu (5ml) denne.
Zloženie: Vysoko purifikovaný rybí olej získaný z celých severských tresiek, organicky viazaný jód. Bez konzervantov, antioxidantov, čistý.
Hmotnosť: 270ml
Jód
Stopové prvky sú nepostrádateľné pre rad fyziologických funkcií. Jód patrí spolu s fluórom, chlórom a brómom do skupiny halogénov, vysoko reaktívnych nekovov. Jód sa najviac prirodzene vyskytuje v morských riasach a morských živočíchoch. Z pohľadu výskytu v prostredí je najmenej zastúpeným halogénom v zemskej kôre. Obsah jódu v pôdach sa líši, väčšinou je relatívne nízky následkom postupného odplavenia do morí.
Jód bol objavený Bernardom Courtoisom v Paríži v roku 1811, ale trvalo takmer 100 rokov kým sa zistila jeho kľúčová úloha pre funkciu štítnej žľazy. V roku 1927 Sir Charles Harrington ohlásil, že veľká časť molekuly tyroxínu (T4 – hormónu štítnej žľazy) bola tvorená jódom (65,3% hmotnosti).
Hlavný význam jódu pre funkciu štítnej žľazy je všeobecne dlhodobo známy, výskumy uskutočnené v posledných niekoľkých rokoch však poodhalili ďalšie funkcie jódu akými sú riadenie metabolizmu takmer každej bunky nášho tela, antioxidačné a antiproliferatívne – proti nádorové účinky. Jód zohráva dôležitú úlohu v prevencii rakoviny prsníka, vaječníkov, prostaty, mozgu, fibrocystického ochorenia prsníka, psychických porúch, deficitu pozornosti, syndrómu hyperaktivity a fibromyalgie.
Jód sa nachádza v potrave vo forme anorganických solí, jodičnanu alebo jodidu, organicky viazaného jódu na bielkoviny, tuky (jódolipidy), v morských riasach (napr. dulse, wakame, kombu) sa nachádza vo forme anorganických diatómických molekúl jódu (molekulárny jód alebo I2) a organického jednoatómového jódu (°I). Jód sa rýchlo vstrebáva do krvného obehu, aktívnym prenosom sa koncentruje vo folikulách štítnej žľazy, kde dosahuje 20-40 násobok koncentrácie v krvi. Okrem štítnej žľazy sa koncentruje v niektorých orgánoch a tkanivách.
U dospelého človeka s primeraným príjmom jódu sa nachádza približne 30% celkového množstva jódu (15 mg) v štítnej žľaze a hormónoch štítnej žľazy, zvyšných 70% (50 mg) sa nachádza extratyroidálne v rôznych tkanivách, najviac sa koncentruje v prsných žľazách, koži, žalúdočnej sliznici, slinných žľazách, maternici, v mozgovo-miešnom likvore.
Fyziologické funkcie jódu
Tyroidálna funkcia – tvorba tyroxínu.
Jód je nevyhnutný pre funkčnosť štítnej žľazy, autoreguláciu a tvorbu hormónov štítnej žľazy, tyroxínu a trijódtyronínu. Je to takzvaná tyriodálna funkcia jódu.
Extratyroidálne funkcie jódu.
Okrem tyriodálnej funkcie zabezpečuje jód množstvo ďalších, takzvaných extratyriodálnych funkcií. Takmer všetky bunky tela majú na povrchu bunkovej steny receptor pre hormóny štítnej žľazy. Jód zapojený do štruktúry hormónov ovplyvňuje prakticky všetky bunky v tele, riadi viacero metabolických funkcií, vrátane bazálnej rýchlosti metabolizmu, metabolizmu bielkovín, tukov a sacharidov, delenie a zánik buniek.
Jód bráni výskytu rakoviny. Kontroluje delenie buniek, rast tkanív. Navodzuje apoptózu – geneticky programovaný zánik buniek. Jód prostredníctvom komunikačných molekúl – jódolaktónov kontroluje signálne mechanizmy buniek sprostredkované rastovými faktormi (VEGF). Protirakovinové účinky jódu sa pokladajú za najvýznamnejšiu extratyroidálnu funkciu jódu.
Antioxidant. Jód je špecifickým antioxidantom vychytávajúcim hydroxylové radikály. Jód chráni mozgové bunky pred peroxidáciou nenasýtených tukov nachádzajúcich sa v bunkových stenách.
20% celkového obsahu sa nachádza v koži, najmä v potných žľazách. Nedostatok jódu spôsobuje suchú kožu so zníženou schopnosťou tvorby potu.
Jód sa sústreďuje tiež v slinných žľazách kde sa zúčastňuje tvorby slín.
Jód sa koncentruje v tkanivách prsnej žľazy, kde pôsobí desenzitizačne na estrogénové receptory, čím dostáva pod kontrolu nadmerné delenie buniek a pôsobí preventívne proti fibrocystickému ochoreniu prsníka a chráni pred vznikom rakoviny prsníka.
V žalúdočnej sliznici zohráva životne dôležitú úlohu pri tvorbe žalúdočnej kyseliny. Nedostatok jódu môže byť príčinou achlórhydrie – poruchy tvorby žalúdočnej kyseliny a môže zvyšovať riziko rakoviny žalúdka. Zvyšuje odolnosť sliznice voči Helicobacter pylori.
》Slzné žľazy potrebujú jód k tvorbe sĺz. Medzi príčiny suchých očí okrem zápalov a nedostatku omega-3 mastných kyselín patrí tiež nedostatok jódu.
》Jód odstraňuje z tela toxické chemikálie a biologické toxíny.
》Potláča auto imunitné procesy.
》Posilňuje T-bunkami sprostredkovanú adaptívnu imunitu.
》Protirakovinové účinky organicky viazaného jódu
Viacero experimentálnych vedeckých štúdií na zvieratách a klinických štúdií u ľudí z obdobia 1993 – 2006 poukázalo na liečebný potenciál molekulárneho jódu (I2) využiteľného v liečbe rakoviny (Ghent et al. 1993, Eskin et al. 1995, Funahashi et al. 1996, Kessler 2004, Garcia-Solis et al. 2005).
V uvedenom období bol objavený mechanizmus pôsobenia jódu a skupina látok nazvaná jódolaktóny.
Čo sú to jódolaktóny?
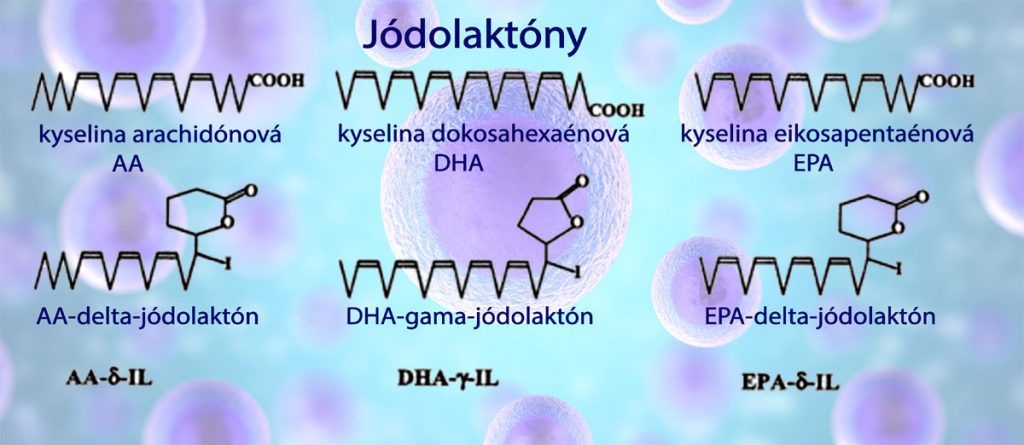
Jódolaktóny patria medzi jódolipidy. Sú to organické zlúčeniny jódu vznikajúce v tele konverziou nenasýtených mastných kyselín a zabudovaním molekúl jódu. Jód sa dokáže v bunkových stenách organicky viazať na nenasýtené mastné kyseliny obsahujúce dvojité väzby, napríklad na kyselinu arachidónovú (AA), kyselinu eikosapentaénovú (omega-3 EPA) a kyselinu dokosahexaénovú (omega-3 DHA) za vzniku takzvaných jódolipidov alebo jódolaktónov.
Jódolaktóny sa zúčastňujú autoregulácie funkcie štítnej žlazy. Opuch, zväčšenie a nadmerná tvorba tyroxínu vzniká pri poruche biologickej kontroly vyplýva z deficitu jódolaktónov. Jódolaktóny obnovujú mechanizmus apoptózy a kontrolujú procesy, aby nedochádzalo k hyperfunkcii alebo hypertrofii tkaniva (zväčšovaniu).
Jódoaktóny na rozdiel od chemoterapie nepôsobia toxicky a nespôsobujú nekrózu zdravých buniek. Pôsobia výlučne fyziologickým mechanizmom indukcie apoptózy. Účinok jódolaktónov je teda vysoko selektívny, nepoškodzuje zdravé tkanivá.
Jódolaktóny majú antiproliferatívny účinok – zabraňujú deleniu rakovinových buniek už vo veľmi nízkych koncentráciách.
Uvedený mechanizmus pôsobenia jódolaktónov je predmetom intenzívneho výskumu pre enormný potenciál pri cielenej liečbe rakoviny.
Doposiaľ boli identifikované viaceré jódolipidy, predmetom záujmu sa však stali najmä delta-jódolaktón (6-IL) a EPA-jódolaktón s preukázaným protirakovinovým pôsobením.
Ako vznikajú jódolaktóny?
Tvorba jódolaktonov prebieha zložitými biochemickými mechanizmami aktívneho prenosu jódu a pôsobením enzýmu peroxidáza na anorganické jodidy. Proces prebieha v bunkových stenách. Najťažšou úlohou enzýmov je rozštiepiť anorganické soli jódu za účelom získania molekúl jódu pre syntézu jódolipidov a jódolaktónov. Uvedené skutočnosti potvrdzujú výsledky štúdií, ktoré poukazujú na chýbajúce antiproliferatívne účinky anorganických foriem jódu.
Po podávaní elementárneho jódu u zvierat aj u ľudí dochádzalo k významnému nárastu tvorby jódolaktónu pozorovateľné obzvlášť v bunkových stenách rakovinových buniek ktoré sú charakteristické až 6-násobne vyššou koncentráciou kyseliny arachidónovej v porovnaní s normálnymi bunkami. Molekulárny jód sa prednostne viaže na kyselinu arachidónovú a vytvára jódolaktóny.
Z experimentálnych štúdií vyplýva, že jódolaktóny vznikajú vo vyššej koncentrácii v prítomnosti molekulárneho jódu (elementárneho jódu – ako I2). Najvyužiteľnejším substrátom – zdrojom pre tvorbu jódolaktónov sú jódolipidy – jódované mastné kyseliny. Jódované mastné kyseliny obsahujú molekuly jódu viazaného organickou väzbou na tuky, ich premena na jódolaktóny je priama aoveľa jednoduchšia a účinnejšia. Príkladom praktického využitia jódolipidov v prevencii a terapii je Rybí olej s organicky viazaným jódom.
Jódolaktóny sa môžu vytvárať v princípe v ktoromkoľvek orgáne pod podmienkou prítomnosti peroxidázy. Ak sa však pristúpi k podávaniu elementárneho jódu alebo organicky viazaného jódu, účinnosť tvorby je niekoľkonásobne vyššia. Prítomnosť peroxidázy nie je potrebná a vznik jódolipidov je v tomto prípade zjednodušený, výsledkom je vyššia koncentrácia jódolaktónov.
| Nutnosť pôsobenia peroxidáz vysvetľuje, prečo podávanie anorganických jodidov vo viacerých prípadoch nedokáže zabezpečiť účinnú koncentráciu jódolaktónov v tkanivách postihnutých tumorom a tým podávanie anorganických jodidov nedokáže navodiť apoptózu – zánik buniek. |
Aké typy jódolaktónov vznikajú v bunkových stenách?
V súčasnosti sú známe jódolaktóny odvodené od polynenasýtených mastných kyselín. AA-delta jódolaktón vytvárajúci sa z kyseliny arachdónovej, EPA-delta jódolaktón vytvárajúci sa z kyseliny eikosapentaénovej a DHA- gama jódolaktón vznikajúci z kyseliny eikosapentaénovej a organického jódu. Proapoptoické, protirakovinové a antiproliferatívne účinky boli dokázané pri AA- a EPA-jódolaktóne. Uvedené typy jódolaktónov dokážu navodiť apoptózu buniek už pri veľmi nízkej koncentrácii 5 mcmol/l. Na obrázku nižšie sú polynenasýtené mastné kyseliny a z nich vzniknuté jódolaktóny.
Experimentálne výsledky: rakovinové bunky sú citlivejšie na molekulárny jód
Podľa výsledkov mexickej štúdie z roku 2008 rakovinové bunky sú oveľa citlivejšie na podávanie molekulárneho jódu (I2) ako normálne bunky. Uvedená hypotéza vychádza z exaktných hodnôt minimálnych koncentrácií, pri ktorých dochádzalo k apoptóze – zániku buniek.
Už relatívne nízke a stredné koncentrácie elementárneho jódu (10 – 20 µM) alebo delta-jódolaktónu (0,5 µM) dokážu navodiť apoptózu rakovinových buniek, zatiaľ čo u normálnych buniek dochádza k navodeniu apoptózy až pri vyššej koncentrácii elementárneho jódu (40 µM).
Výsledky potvrdzujú že rovnako elementárny jód ako aj delta-jódolaktón aktivujú rovnaký intracelulárny (vnútrobunkový) mechanizmus.
Antineoplastické – protirakovinové účinky zahŕňajú väzbu elementárneho jódu na kyselinu arachidónovú, eikosapentaénovú a vznik delta-jódolaktónov.
Zdroje:
O.Arroyo-Helguera, E Rojas,G.Delgado,C.Aceves: Signaling pathways involved in the antiproliferative effect of molecular iodine in normal and tumoral breast cells: evidence that 6-iodolactone mediates apoptotic effects; Endoc.Cancer 2008;15:1003
C.Aceves et al:Antineoplastic effect of iodine in mammary cancer: participation of 6-iodolactone (6-IL) and peroxisome proliferator-activated receptors (PPAR); Mol.Cancer 2009; 8:33
Cytotoxická aktivita molekulárneho jódu a jódolaktónov testovaná na 12 rozličných typoch izolovaných ľudských rakovinových buniek. Dôkaz o indukcii apoptózy bez ovplyvnenie EGF-signálnej cesty.
Cytotoxický a antiproliferatívny potenciál (zastavujúci delenie buniek) molekulárneho jódu a jódolaktónov bol skúmaný na 12 rôznych typoch izolovaných ľudských rakovinových buniek a jednom type normálnych buniek. S výnimkou rakovinových buniek hrubého čreva (CCL221) sa rast všetkých ďalších 11 typov rakovinových buniek spomalil, ak tieto bunky boli vystavené pôsobeniu molekulárneho jódu v koncentrácii 10 microM počas najmenej 2 dní. Delta-jódolaktón mal v koncentrácii 5 mikroM podobné účinky.
Najcitlivejšie na účinky molekulárneho jódu a delta-jódolaktónu sa ukázali bunky neuroblastómu (SH-SY5Y), ďalej bunky karcinómu prsníka (MCF-7) s mierou inhibície 60% a 77,7% a bunky karcinómu pľúc 36,3% a 40,3%. V protiklade s účinkami na rakovinových bunkách, normálne epitelové bunky prsníka boli podstatne menej citlivé na účinky jódu.
Pri typoch buniek SH-SY5Y a MCF-7 molekulový jód a jódolaktón úplne zrušil EGF faktorom zapríčinené delenie buniek.
Prerušenie delenia buniek však nebolo spôsobené zasiahnutím EGF signálnej cesty pretože I2 a IL neovplyvnili fosforyláciu EGF-receptora ani EGF-indukovanú aktiváciu MAP-kinázy.
Prerušenie delenia molekulárnym jódom bolo možne eliminovať prítomnosťou N-acetylcysteínu, z čoho vyplýva že jód (I2) aktivuje mitochondriálny mechanizmus apoptózy buniek.
Zdroj: Rösner H, Torremante P, Möller W, Gärtner R.: Antiproliferative/cytotoxic activity of molecular iodine and iodolactones in various human carcinoma cell lines. No interfering with EGF-signaling, but evidence for apoptosis; Exp Clin Endocrinol Diabetes. 2010 Jul;118(7):410-9.
Jódolaktóny sú signálne molekuly. Majú schopnosť navodiť apoptózu – geneticky programovaný zánik buniek. Apoptóza je veľmi dôležitý mechanizmus kontroly delenia buniek, zúčastňuje sa reparačných mechanizmov, odstráňovania poškodených buniek a tkanív. Rakovinové bunky strácajú schopnosť apoptózy, čo umožňuje neobmedzené, nekontrolované delenie.
Jódolaktóny sa zúčastňujú autoregulácie funkcie štítnej žlazy. Opuch, zväčšenie a nadmerná tvorba tyroxínu vzniká pri poruche biologickej kontroly vyplýva z deficitu jódolaktónov. Jódolaktóny obnovujú mechanizmus apoptózy a kontrolujú procesy, aby nedochádzalo k hyperfunkcii alebo hypertrofii tkaniva (zväčšovaniu).
Jódoaktóny na rozdiel od chemoterapie nepôsobia toxicky a nespôsobujú nekrózu zdravých buniek. Pôsobia výlučne fyziologickým mechanizmom indukcie apoptózy. Účinok jódolaktónov je teda vysoko selektívny, nepoškodzuje zdravé tkanivá.
Jódolaktóny majú antiproliferatívny účinok – zabraňujú deleniu rakovinových buniek už vo veľmi nízkych koncentráciách.
Uvedený mechanizmus pôsobenia jódolaktónov je predmetom intenzívneho výskumu pre enormný potenciál pri cielenej liečbe rakoviny.
Doposiaľ boli identifikované viaceré jódolipidy, predmetom záujmu sa však stali najmä delta-jódolaktón (6-IL) a EPA-jódolaktón s preukázaným protirakovinovým pôsobením.
Ako vznikajú jódolaktóny?
Tvorba jódolaktonov prebieha zložitými biochemickými mechanizmami aktívneho prenosu jódu a pôsobením enzýmu peroxidáza na anorganické jodidy. Proces prebieha v bunkových stenách. Najťažšou úlohou enzýmov je rozštiepiť anorganické soli jódu za účelom získania molekúl jódu pre syntézu jódolipidov a jódolaktónov. Uvedené skutočnosti potvrdzujú výsledky štúdií, ktoré poukazujú na chýbajúce antiproliferatívne účinky anorganických foriem jódu.
Po podávaní elementárneho jódu u zvierat aj u ľudí dochádzalo k významnému nárastu tvorby jódolaktónu pozorovateľné obzvlášť v bunkových stenách rakovinových buniek ktoré sú charakteristické až 6-násobne vyššou koncentráciou kyseliny arachidónovej v porovnaní s normálnymi bunkami. Molekulárny jód sa prednostne viaže na kyselinu arachidónovú a vytvára jódolaktóny.
Z experimentálnych štúdií vyplýva, že jódolaktóny vznikajú vo vyššej koncentrácii v prítomnosti molekulárneho jódu (elementárneho jódu – ako I2). Najvyužiteľnejším substrátom – zdrojom pre tvorbu jódolaktónov sú jódolipidy – jódované mastné kyseliny. Jódované mastné kyseliny obsahujú molekuly jódu viazaného organickou väzbou na tuky, ich premena na jódolaktóny je priama aoveľa jednoduchšia a účinnejšia. Príkladom praktického využitia jódolipidov v prevencii a terapii je Rybí olej s organicky viazaným jódom.
Jódolaktóny sa môžu vytvárať v princípe v ktoromkoľvek orgáne pod podmienkou prítomnosti peroxidázy. Ak sa však pristúpi k podávaniu elementárneho jódu alebo organicky viazaného jódu, účinnosť tvorby je niekoľkonásobne vyššia. Prítomnosť peroxidázy nie je potrebná a vznik jódolipidov je v tomto prípade zjednodušený, výsledkom je vyššia koncentrácia jódolaktónov.
| Nutnosť pôsobenia peroxidáz vysvetľuje, prečo podávanie anorganických jodidov vo viacerých prípadoch nedokáže zabezpečiť účinnú koncentráciu jódolaktónov v tkanivách postihnutých tumorom a tým podávanie anorganických jodidov nedokáže navodiť apoptózu – zánik buniek. |
Aké typy jódolaktónov vznikajú v bunkových stenách?
V súčasnosti sú známe jódolaktóny odvodené od polynenasýtených mastných kyselín. AA-delta jódolaktón vytvárajúci sa z kyseliny arachdónovej, EPA-delta jódolaktón vytvárajúci sa z kyseliny eikosapentaénovej a DHA- gama jódolaktón vznikajúci z kyseliny eikosapentaénovej a organického jódu. Proapoptoické, protirakovinové a antiproliferatívne účinky boli dokázané pri AA- a EPA-jódolaktóne. Uvedené typy jódolaktónov dokážu navodiť apoptózu buniek už pri veľmi nízkej koncentrácii 5 mcmol/l. Na obrázku nižšie sú polynenasýtené mastné kyseliny a z nich vzniknuté jódolaktóny.
Experimentálne výsledky: rakovinové bunky sú citlivejšie na molekulárny jód
Podľa výsledkov mexickej štúdie z roku 2008 rakovinové bunky sú oveľa citlivejšie na podávanie molekulárneho jódu (I2) ako normálne bunky. Uvedená hypotéza vychádza z exaktných hodnôt minimálnych koncentrácií, pri ktorých dochádzalo k apoptóze – zániku buniek.
Už relatívne nízke a stredné koncentrácie elementárneho jódu (10 – 20 µM) alebo delta-jódolaktónu (0,5 µM) dokážu navodiť apoptózu rakovinových buniek, zatiaľ čo u normálnych buniek dochádza k navodeniu apoptózy až pri vyššej koncentrácii elementárneho jódu (40 µM).
Výsledky potvrdzujú že rovnako elementárny jód ako aj delta-jódolaktón aktivujú rovnaký intracelulárny (vnútrobunkový) mechanizmus.
Antineoplastické – protirakovinové účinky zahŕňajú väzbu elementárneho jódu na kyselinu arachidónovú, eikosapentaénovú a vznik delta-jódolaktónov.
Zdroje:
1O.Arroyo-Helguera, E Rojas,G.Delgado,C.Aceves: Signaling pathways involved in the antiproliferative effect of molecular iodine in normal and tumoral breast cells: evidence that 6-iodolactone mediates apoptotic effects; Endoc.Cancer 2008;15:1003
C.Aceves et al:Antineoplastic effect of iodine in mammary cancer: participation of 6-iodolactone (6-IL) and peroxisome proliferator-activated receptors (PPAR); Mol.Cancer 2009; 8:33
Cytotoxická aktivita molekulárneho jódu a jódolaktónov testovaná na 12 rozličných typoch izolovaných ľudských rakovinových buniek. Dôkaz o indukcii apoptózy bez ovplyvnenie EGF-signálnej cesty.
Cytotoxický a antiproliferatívny potenciál (zastavujúci delenie buniek) molekulárneho jódu a jódolaktónov bol skúmaný na 12 rôznych typoch izolovaných ľudských rakovinových buniek a jednom type normálnych buniek. S výnimkou rakovinových buniek hrubého čreva (CCL221) sa rast všetkých ďalších 11 typov rakovinových buniek spomalil, ak tieto bunky boli vystavené pôsobeniu molekulárneho jódu v koncentrácii 10 microM počas najmenej 2 dní. Delta-jódolaktón mal v koncentrácii 5 mikroM podobné účinky.
Najcitlivejšie na účinky molekulárneho jódu a delta-jódolaktónu sa ukázali bunky neuroblastómu (SH-SY5Y), ďalej bunky karcinómu prsníka (MCF-7) s mierou inhibície 60% a 77,7% a bunky karcinómu pľúc 36,3% a 40,3%. V protiklade s účinkami na rakovinových bunkách, normálne epitelové bunky prsníka boli podstatne menej citlivé na účinky jódu.
Pri typoch buniek SH-SY5Y a MCF-7 molekulový jód a jódolaktón úplne zrušil EGF faktorom zapríčinené delenie buniek.
Prerušenie delenia buniek však nebolo spôsobené zasiahnutím EGF signálnej cesty pretože I2 a IL neovplyvnili fosforyláciu EGF-receptora ani EGF-indukovanú aktiváciu MAP-kinázy.
Prerušenie delenia molekulárnym jódom bolo možne eliminovať prítomnosťou N-acetylcysteínu, z čoho vyplýva že jód (I2) aktivuje mitochondriálny mechanizmus apoptózy buniek.
Zdroj: Rösner H, Torremante P, Möller W, Gärtner R.: Antiproliferative/cytotoxic activity of molecular iodine and iodolactones in various human carcinoma cell lines. No interfering with EGF-signaling, but evidence for apoptosis; Exp Clin Endocrinol Diabetes. 2010 Jul;118(7):410-9.
Podávaním anorganických solí jódu nedochádza k výraznejšiemu zvýšeniu tvorby jódolaktónov. Anorganické soli jódu preto nevykazujú antiproliferatívne (protirakovinové) účinky.
Podávanie jódu viazaného organickou väzbou na viacnenasýtené mastné kyseliny (tuky) je vysoko účinný spôsob zabezpečenia zvýšenej tvorby jódolaktónov v tele.
Zvýšenie tvorby jódolaktónov umožňuje opätovnú obnovu kontroly delenia buniek, potláča rast nádorov, obnovuje autoreguláciu činnosti štítnej žlazy, obmedzuje tvorbu cýst v materrnici a prsnej žľaze, bráni hypertrofii prostaty.
Viete, ako sa zbaviť cysty? Indol3C je riešením aj na tento problém. Prečítajte si viac v našom článku: Ako sa zbaviť cysty?




















Zákazník (overený zákazník) –
Zákazník (overený zákazník) –
Zákazník (overený zákazník) –
Tento produkt ja používam u dlhé roky a som veľmi spokojná
Zákazník (overený zákazník) –
Zákazník (overený zákazník) –
Zákazník –
obcas zabudam uzit, kedze musi byt v chladnicke a musi sa pocas jedla uzivat
Zákazník (overený zákazník) –
Vsetko prebehlo v poriadku, tovar doruceny neposkodeny a rychlo.
Zákazník (overený zákazník) –
Perfektny!
Zákazník (overený zákazník) –
Som spokojná